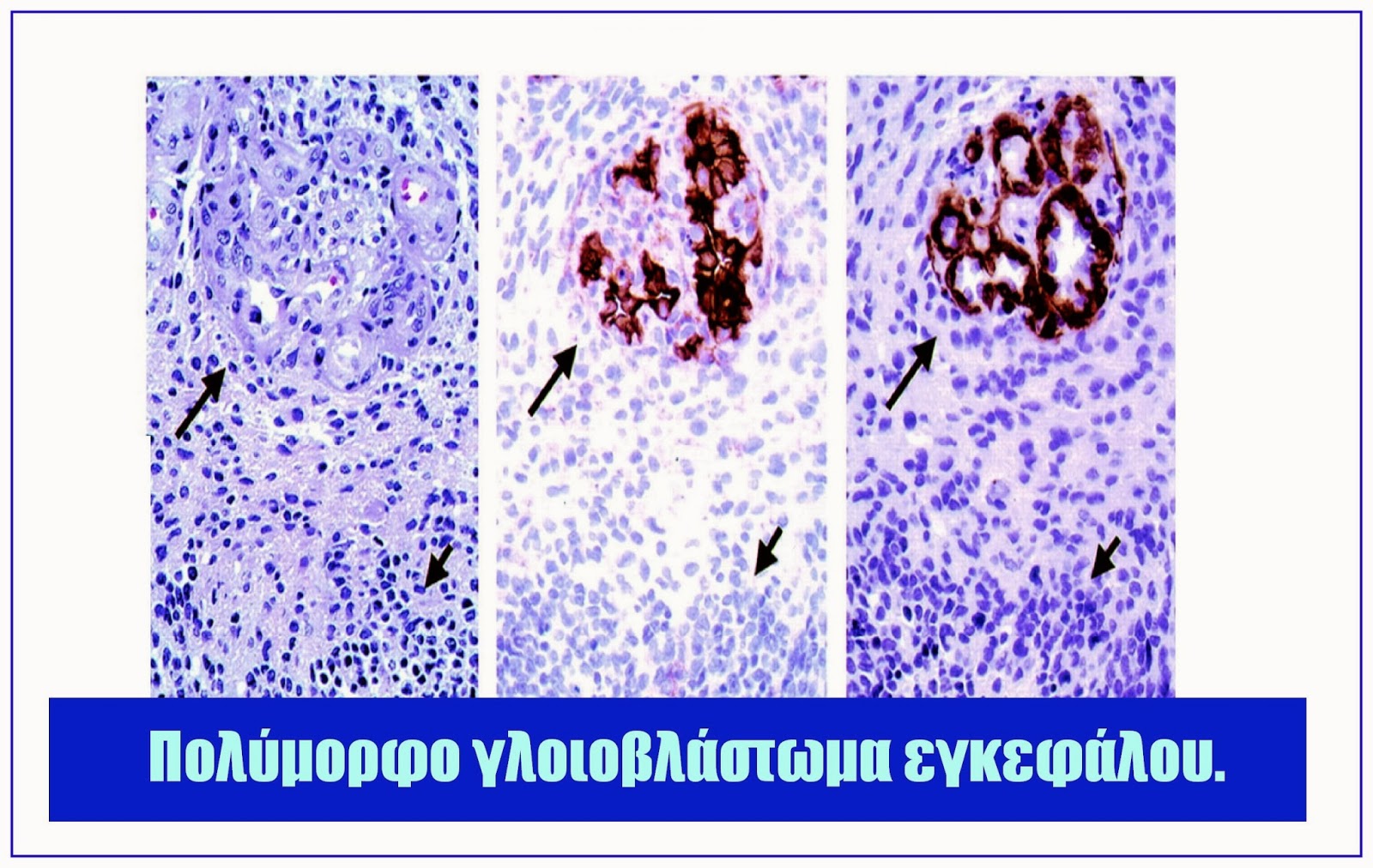
Το Πολύμορφο Γλοιοβλάστωμα (Glioblastoma multiforme-GBM) είναι ο πιο κοινός και δυστυχώς ο πιο επιθετικός και κακοήθης τύπος πρωτοπαθούς εγκεφαλικού όγκου στους ανθρώπους, αποτελώντας το 52% όλων των περιπτώσεων ενδοπαρεγχυματικών εγκεφαλικών όγκων και το 20% όλων των ενδοκρανιακών όγκων. Σύμφωνα με την ταξινόμηση των όγκων του κεντρικού νευρικού συστήματος από τον Παγκόσμιο Οργανισμό Υγείας, ο καθιερωμένος όρος γι' αυτό τον εγκεφαλικό όγκο είναι "γλοιοβλάστωμα", ενώ εμφανίζει δύο μορφές: το γιγαντοκυτταρικό γλοιοβλάστωμα και το γλοιοσάρκωμα. Η συχνότητα εμφάνισης του φτάνει περίπου τα 5 νέα περιστατικά/100.000 ανθρώπων, ανά έτος. Το κλινικό ιστορικό των ασθενών με πολύμορφο γλοιοβλάστωμα είναι συνήθως μικρό (λιγότερο από 3 μήνες σε ποσοστό άνω του 50% των ασθενών) καθώς ο όγκος αυτός εμφανίζει μεγάλη επιθετικότητα και γρήγορη αύξηση. Η πρόγνωση του δε είναι από τις χειρότερες στην σύγχρονη ιατρική: η διάμεση επιβίωση των ασθενών με γλοιοβλάστωμα με δυσκολία ξεπερνά τους 12 μήνες, παρά τις σύγχρονες εξελίξεις στην νευροχειρουργική και την νευρο-ογκολογία.
Το πολύμορφο γλοιοβλάστωμα ανήκει στην κατηγορία των πρωτογενών-πρωτοπαθών όγκων του εγκεφάλου. Αυτό σημαίνει ότι αναπτύσσεται από κύτταρα που βρίσκονται στον εγκέφαλο και δεν είναι αποτέλεσμα μετάστασης άλλων καρκίνων από διαφορετικές περιοχές του σώματος. Οι πρωτογενείς όγκοι του εγκεφάλου είναι σπανιότεροι από τους μεταστατικούς όγκους του εγκεφάλου. Έχουν περιγραφεί 120 διαφορετικοί τύποι όγκων που εμφανίζονται στον εγκέφαλο. Οι πρωτογενείς όγκοι του εγκεφάλου προσβάλλουν περίπου 14 σε κάθε 100.000 ανθρώπους κάθε χρόνο. Μπορεί να είναι καλοήθεις ή κακοήθεις. Σε 7 περιπτώσεις ανά 100.000 είναι κακοήθεις όγκοι. Η συχνότερη μορφή πρωτογενούς όγκου του εγκεφάλου είναι το γλοίωμα (49%) και ακολουθεί το μηνιγγίωμα (30%) που είναι καλοήθης όγκος. Οι πρωτογενείς όγκοι εγκεφάλου μπορούν να εκδηλωθούν σε οποιαδήποτε ηλικία. Ωστόσο η συχνότητα τους είναι μεγαλύτερη σε παιδιά ηλικίας 3 έως 12 ετών και σε ενήλικες 40 έως 70 ετών.
Μεταξύ των πρωτογενών/πρωτοπαθών καρκίνων του εγκεφάλου η μεγαλύτερη ομάδα είναι τα γλοιώματα. Τα γλοιώματα είναι όγκοι στον εγκέφαλο που αναπτύσσονται από τα νευρογλοιακά κύτταρα, τα κύτταρα δηλαδή που "στηρίζουν" και "τρέφουν" τους νευρώνες του εγκεφάλου.
Τα γλοιώματα ταξινομούνται ανάλογα με τον τύπο των κυττάρων από τα οποία αποτελούνται αλλά και με βάση τον βαθμό κακοήθειάς τους.
Τα γλοιώματα ταξινομούνται σύμφωνα με τον συγκεκριμένο τύπο του κυττάρου που μοιράζονται με ιστολογικά χαρακτηριστικά, αλλά χωρίς απαραιτήτως να προέρχονται κι από αυτά. Οι κύριοι τύποι των γλοιωμάτων είναι οι εξής:
*Επενδυμώματα-προέρχονται από επενδυματικά κύτταρα.
*Αστροκυτώματα-προέρχονται από αστροκύτταρα (το πολύμορφο γλοιοβλάστωμα είναι το πιο κοινό σε αυτήν την κατηγορία).
*Ολιγοδενδρογλοιώματα-προέρχονται από τα ολιγοδενδροκύτταρα.
*Μικτά γλοιώματα, όπως ολιγοαστροκυττώματα, περιέχουν κύτταρα από διαφορετικούς τύπους νευρογλοίας.
Η κάθε κατηγορία από τις παραπάνω έχει υποκατηγορίες ανάλογα πάλι με την προέλευση των κυττάρων.
Τα γλοιώματα περαιτέρω κατηγοριοποιούνται ανάλογα με βαθμό κακοήθειάς τους η οποία καθορίζεται από την ιστοπαθολογική εξέταση του όγκου.
Από τα πολυάριθμα συστήματα ταξινόμησης των γλοιωμάτων, το πιο κοινό σύστημα ταξινόμησης για αστροκυτώματα είναι της Παγκόσμιας Οργάνωσης Υγείας (ΠΟΥ), σύμφωνα με την οποία οι όγκοι βαθμολογούνται από Ι (Χαμηλού βαθμού κακοήθειας - υψηλής διαφοροποίησης γλοίωμα: λιγότερο προχωρημένη νόσος-καλύτερη πρόγνωση) έως IV (Υψηλού βαθμού κακοήθειας - χαμηλής διαφοροποίησης γλοίωμα: πιο προχωρημένο στάδιο της νόσου-χειρότερη πρόγνωση).
• Αστροκύτωμα grade 1 κατά WHO (πιλοκυτταρικό αστροκύτωμα).
• Αστροκύτωμα grade 2 κατά WHO
• Αστροκύτωμα grade 3 κατά WHO (αναπλαστικό αστροκύτωμα)
• Αστροκύτωμα grade 4 κατά WHΟ (πολύμορφο γλοιοβλάστωμα).
Τα γλοιώματα ταξινομούνται ανάλογα με τον τύπο των κυττάρων από τα οποία αποτελούνται αλλά και με βάση τον βαθμό κακοήθειάς τους.
Τα γλοιώματα ταξινομούνται σύμφωνα με τον συγκεκριμένο τύπο του κυττάρου που μοιράζονται με ιστολογικά χαρακτηριστικά, αλλά χωρίς απαραιτήτως να προέρχονται κι από αυτά. Οι κύριοι τύποι των γλοιωμάτων είναι οι εξής:
*Επενδυμώματα-προέρχονται από επενδυματικά κύτταρα.
*Αστροκυτώματα-προέρχονται από αστροκύτταρα (το πολύμορφο γλοιοβλάστωμα είναι το πιο κοινό σε αυτήν την κατηγορία).
*Ολιγοδενδρογλοιώματα-προέρχονται από τα ολιγοδενδροκύτταρα.
*Μικτά γλοιώματα, όπως ολιγοαστροκυττώματα, περιέχουν κύτταρα από διαφορετικούς τύπους νευρογλοίας.
Η κάθε κατηγορία από τις παραπάνω έχει υποκατηγορίες ανάλογα πάλι με την προέλευση των κυττάρων.
Τα γλοιώματα περαιτέρω κατηγοριοποιούνται ανάλογα με βαθμό κακοήθειάς τους η οποία καθορίζεται από την ιστοπαθολογική εξέταση του όγκου.
Από τα πολυάριθμα συστήματα ταξινόμησης των γλοιωμάτων, το πιο κοινό σύστημα ταξινόμησης για αστροκυτώματα είναι της Παγκόσμιας Οργάνωσης Υγείας (ΠΟΥ), σύμφωνα με την οποία οι όγκοι βαθμολογούνται από Ι (Χαμηλού βαθμού κακοήθειας - υψηλής διαφοροποίησης γλοίωμα: λιγότερο προχωρημένη νόσος-καλύτερη πρόγνωση) έως IV (Υψηλού βαθμού κακοήθειας - χαμηλής διαφοροποίησης γλοίωμα: πιο προχωρημένο στάδιο της νόσου-χειρότερη πρόγνωση).
• Αστροκύτωμα grade 1 κατά WHO (πιλοκυτταρικό αστροκύτωμα).
• Αστροκύτωμα grade 2 κατά WHO
• Αστροκύτωμα grade 3 κατά WHO (αναπλαστικό αστροκύτωμα)
• Αστροκύτωμα grade 4 κατά WHΟ (πολύμορφο γλοιοβλάστωμα).
Οι βαθμοί αντικατοπτρίζουν πρακτικά την επιθετικότητα των όγκων αυτών. Ενώ το πιλοκυταρικό αστροκύτωμα δεν έχει την προδιάθεση να εξελίσσεται επιθετικά και η πλήρης εξαίρεσή του συνεπάγεται και πλήρη ίαση, δε συμβαίνει το ίδιο στους βαθμούς 2-4. Οι όγκοι 2ου βαθμού χαρακτηρίζονται ως χαμηλής κακοήθειας αστροκυτώματα. Σε βάθος χρόνου όμως εξελίσσονται στις πιο κακοήθεις μορφές 3 και 4. Ο μέσος όρος επιβίωσης εξαρτάται από την ηλικία, το μέγεθος και την εντόπιση του όγκου και κυμαίνεται από 5-15 έτη. Το αναπλαστικό αστροκύτωμα 3ου βαθμού, αναπτύσσεται σαφώς πιο επιθετικά και σε συντομότερο χρονικό διάστημα, με μέσο όρο επιβίωσης από 0,5 έως 3 έτη. Το γλοιοβλάστωμα, που είναι και η συχνότερη μορφή γλοιώματος, έχει ταχύτατη εξέλιξη και τον χαμηλότερο μέσο όρο επιβίωσης (0,5-1 έτος). Το γλοίωμα χαμηλής κακοήθειας εμφανίζεται συνήθως σε νέους ανθρώπους, ακόμα και σε παιδιά. (μέσος όρος ηλικίας είναι τα 34 χρόνια). Συγκριτικά τα αστροκυτώματα υψηλής κακοήθειας εμφανίζονται σε ανθρώπους μεγαλύτερης ηλικίας. Ο μέσος όρος ηλικίας είναι 41 χρόνια για το αναπλαστικό αστροκύτωμα και 53 χρόνια για το πολύμορφο γλοιοβλάστωμα.
Το πολύμορφο γλοιοβλάστωμα εμφανίζεται γενικά σε μέσης και μεγάλης ηλικίας ανθρώπους, ηλικίας 45-70 ετών. Ωστόσο μπορεί να εμφανιστεί σε κάθε ηλικία, ακόμα και σε παιδιά. Ευτυχώς μόνο το τρία τοις εκατό των όγκων του εγκεφάλου παιδικής ηλικίας είναι γλοιοβλαστώματα. Στον γενικό πληθυσμό αναφέρονται 5 νέα περιστατικά ανά 100.000 πληθυσμού, ανά έτος. Ο όγκος αυτός αντιπροσωπεύει περίπου το 17-20 % του συνόλου των πρωτογενών όγκων του εγκεφάλου και περίπου 60-75% του συνόλου των αστροκυτωμάτων. Φαίνεται να επηρεάζει περισσότερο τους άνδρες από τις γυναίκες. Ανάλογα με τον μηχανισμό παθογένειας αναγνωρίζονται δύο είδη γλοιοβλαστώματος:
1) το "πρωτοπαθές" γλοιοβλάστωμα (60% των περιπτώσεων) είναι ταχύτατης εξέλιξης κακοήθης όγκος που εμφανίζεται σε ανθρώπους ηλικίας άνω των 50 ετών, de novo δηλ. χωρίς να υπάρχει προγενέστερη μορφή του όγκου.
2) το "δευτεροπαθές" γλοιοβλάστωμα (40% των περιπτώσεων) προκαλείται από εξαλλαγή ενός χαμηλής κακοήθειας αστροκυτώματος, αφορά σε νέους ανθρώπους και έχει ένα διαφορετικό φάσμα γενετικών αλλαγών, δηλαδή διαφορετικό μοριακό προφίλ από το πρωτοπαθές γλοιοβλάστωμα.
Δύο άλλες μορφές, το πολυεστιακό πολύμορφο γλοιοβλάστωμα και η εγκεφαλική γλοιωμάτωση (Gliomatosis cerebri) θεωρούνται ξεχωριστές νοσολογικές οντότητες.
Δύο άλλες μορφές, το πολυεστιακό πολύμορφο γλοιοβλάστωμα και η εγκεφαλική γλοιωμάτωση (Gliomatosis cerebri) θεωρούνται ξεχωριστές νοσολογικές οντότητες.
Το πολύμορφο γλοιοβλάστωμα χαρακτηρίζεται από την παρουσία μικρών περιοχών νεκρωτικού ιστού που περιβάλλεται από αναπλαστικά κύτταρα. Το χαρακτηριστικό αυτό, καθώς και η παρουσία των υπερπλαστικών αιμοφόρων αγγείων, διαφοροποιεί τον όγκο από τα αστροκυττώματα βαθμού 3, τα οποία δεν έχουν αυτά τα χαρακτηριστικά.
Τα συμπτώματα των γλοιωμάτων εξαρτώνται από το ποιο τμήμα του κεντρικού νευρικού συστήματος έχει επηρεαστεί. Γενικά τα υπερσκηνίδια νεοπλάσματα εκδηλώνονται με διάφορα κλινικά συμπτώματα τα οποία μπορούν να ταξινομηθούν σε 4 κλινικά σύνδρομα:
1. Αύξηση ενδοκρανίου πιέσεως.
2. Εστιακές νευρολογικές εκδηλώσεις.
3. Διαταραχές ανωτέρων ψυχικών λειτουργιών και ειδικά σύνδρομα των λοβών του εγκεφάλου.
4. Συστηματικές διαταραχές.
Παρόλο που στα κοινά συμπτώματα της ασθένειας περιλαμβάνονται οι επιληπτικές κρίσεις, η ναυτία, οι έμετοι, οι πονοκέφαλοι και η ημιπάρεση, κυριότερο σύμπτωμα αποτελεί συνήθως μια προοδευτική αλλοίωση της μνήμης και της προσωπικότητας, λόγω της εμπλοκής των κροταφικών και μετωπιαίων λοβών, καθώς αυτοί οι λοβοί είναι και οι πιο συχνές θέσεις εντόπισής τους. Το είδος των εμφανιζομένων συμπτωμάτων εξαρτάται κατά κύριο λόγο από τη θέση του όγκου και λιγότερο από τα παθολογικά χαρακτηριστικά του. Ο όγκος μπορεί να οδηγήσει στην εμφάνιση συμπτωμάτων γρήγορα, αλλά περιστασιακά παρατηρείται ασυμπτωματική κατάσταση, μέχρις ότου αποκτήσει μεγάλες διαστάσεις. Λόγω της ταχείας ανάπτυξής του, τα συμπτώματα του πολύμορφου γλοιοβλαστώματος συνήθως αναπτύσσονται γρήγορα μέσα σε λίγες εβδομάδες ή μήνες. Εστιακά νευρολογικά ελλείμματα, όπως η παράλυση, η αφασία και οι διαταραχές της όρασης μπορούν να προστεθούν στα συμπτώματα ανάλογα με τον εντοπισμό. Τέλος, υπάρχουν συχνά εντυπωσιακές αλλαγές της προσωπικότητας, απάθεια και ψυχοκινητική καθυστέρηση, τα οποία οδηγούν τον ασθενή στο γιατρό. Συμπτώματα ενδοκρανιακής υπέρτασης όπως οίδημα οπτικής θηλής, έμετος, υπνηλία και κώμα συμβαίνουν αργότερα και είναι δυσμενείς προγνωστικοί δείκτες.
1. Αύξηση ενδοκρανίου πιέσεως.
2. Εστιακές νευρολογικές εκδηλώσεις.
3. Διαταραχές ανωτέρων ψυχικών λειτουργιών και ειδικά σύνδρομα των λοβών του εγκεφάλου.
4. Συστηματικές διαταραχές.
Παρόλο που στα κοινά συμπτώματα της ασθένειας περιλαμβάνονται οι επιληπτικές κρίσεις, η ναυτία, οι έμετοι, οι πονοκέφαλοι και η ημιπάρεση, κυριότερο σύμπτωμα αποτελεί συνήθως μια προοδευτική αλλοίωση της μνήμης και της προσωπικότητας, λόγω της εμπλοκής των κροταφικών και μετωπιαίων λοβών, καθώς αυτοί οι λοβοί είναι και οι πιο συχνές θέσεις εντόπισής τους. Το είδος των εμφανιζομένων συμπτωμάτων εξαρτάται κατά κύριο λόγο από τη θέση του όγκου και λιγότερο από τα παθολογικά χαρακτηριστικά του. Ο όγκος μπορεί να οδηγήσει στην εμφάνιση συμπτωμάτων γρήγορα, αλλά περιστασιακά παρατηρείται ασυμπτωματική κατάσταση, μέχρις ότου αποκτήσει μεγάλες διαστάσεις. Λόγω της ταχείας ανάπτυξής του, τα συμπτώματα του πολύμορφου γλοιοβλαστώματος συνήθως αναπτύσσονται γρήγορα μέσα σε λίγες εβδομάδες ή μήνες. Εστιακά νευρολογικά ελλείμματα, όπως η παράλυση, η αφασία και οι διαταραχές της όρασης μπορούν να προστεθούν στα συμπτώματα ανάλογα με τον εντοπισμό. Τέλος, υπάρχουν συχνά εντυπωσιακές αλλαγές της προσωπικότητας, απάθεια και ψυχοκινητική καθυστέρηση, τα οποία οδηγούν τον ασθενή στο γιατρό. Συμπτώματα ενδοκρανιακής υπέρτασης όπως οίδημα οπτικής θηλής, έμετος, υπνηλία και κώμα συμβαίνουν αργότερα και είναι δυσμενείς προγνωστικοί δείκτες.
Ο όγκος μπορεί να επεκταθεί στις μήνιγγες ή τις κοιλίες του εγκεφάλου, με αποτέλεσμα υψηλή περιεκτικότητα πρωτεϊνών στο εγκεφαλονωτιαίο υγρό (ΕΝΥ) (>100 mg/dL), καθώς και μια περιστασιακή πλειοκυττάρωση από 10 έως 100 κύτταρα, κυρίως λεμφοκύτταρα. Κακοήθη κύτταρα μεταφέρονται στο ΕΝΥ και η νόσος μπορεί να εξαπλωθεί (σπάνια) στο νωτιαίο μυελό ή να προκαλέσει μηνιγγική γλοιωμάτωση. Ωστόσο, μετάσταση του πολύμορφου γλοιοβαστώματος πέρα από το κεντρικό νευρικό σύστημα είναι ανύπαρκτη.
Περίπου το 50% των Πολύμορφων Γλοιοβλαστωμάτων καταλαμβάνουν περισσότερους από έναν λοβούς του ενός ημισφαιρίου ή εντοπίζονται ακόμη και στα δύο εγκεφαλικά ημισφαίρια την στιγμή της διάγνωσής τους. Το Πολύμορφο Γλοιοβλάστωμα συνήθως αναπτύσσεται στους λοβούς των εγκεφαλικών ημισφαιρίων, με υπεροχή κατά σειρά στον κροταφικό, τον βρεγματικό και το μετωπιαίο λοβό, παρότι μπορεί να εντοπίζεται σε οποιοδήποτε λοβό. Μπορεί να εντοπίζεται στα βασικά γάγγλια και σπάνια στον οπίσθιο κρανιακό βόθρο. Έχει την τάση να επεκτείνεται κατά μήκος των οδών της λευκής ουσίας, όπως το μεσολόβιο, η έσω κάψα, η οπτική ακτινοβολία, ο πρόσθιος σύνδεσμος, η ψαλίδα και οι υποεπενδυματικές ζώνες. Τέτοιου είδους επεκτάσεις μπορούν να δημιουργήσουν την εικόνα του πολυεστιακού γλοιοβλαστώματος. Στην πραγματικότητα, όπως αποδεικνύει η ιστοπαθολογική εξέταση σε νεκροτομικά παρασκευάσματα, ένα μικρό ποσοστό της τάξεως του 2–7% των γλοιοβλαστωμάτων αφορούν πολλαπλούς ανεξάρτητους όγκους και όχι απομακρυσμένες επεκτάσεις ενός αρχικού όγκου. Η διάγνωση γίνεται με την αξονική και μαγνητική τομογραφία, στις οποίες απαιτείται πάντα η χρήση ενδοφλέβιου σκιαγραφικού. Ο όγκος μπορεί να λάβει μία ποικιλία εμφανίσεων, ανάλογα με την ποσότητα της αιμορραγίας, της νέκρωσης, και της ηλικίας του. Στην αξονική τομογραφία το γλοιοβλάστωμα εμφανίζεται ως μάζα κεντρικά υπόπυκνη, με έντονο ανομοιογενή περιφερικό εμπλουτισμό, ο οποίος είναι συνήθως παχύς και οζώδης. Χαρακτηριστική είναι και η παρουσία οιδήματος το οποίο περιβάλει τη βλάβη και προκαλεί πιεστικά φαινόμενα, και έτσι μπορεί να συμπιέσει τις κοιλίες και να προκαλέσει υδροκέφαλο. Η μαγνητική τομογραφία (MRI – magnetic resonance imaging) είναι η εξέταση εκλογής για το Πολύμορφο Γλοιοβλάστωμα. Στην ακολουθία Τ1 εμφανίζεται ως περιοχή με χαμηλό ή μικτό σήμα και μετά τη χορήγηση παραμαγνητικής ουσίας παρατηρείται έντονος ανομοιογενής, πολλές φορές δακτυλιοειδής, περιφερικός εμπλουτισμός. Αντίθετα με την παλαιότερη άποψη ότι ο εμπλουτισμός αποτελούσε το έξω όριο του όγκου, έχει καταδειχθεί από διάφορες παθολογοανατομικές μελέτες ότι αυτό δεν είναι αληθές, καθώς νεοπλασματικά κύτταρα μπορούν εύκολα να αναγνωριστούν σε απόσταση 2 cm από το όριο του εμπλουτισμού. Το κεντρικό χαμηλό σήμα αντιστοιχεί στη περιοχή της νέκρωσης του όγκου. Στην ακολουθία ακολουθία Τ2 το περιβάλλον αγγειογενές οίδημα εμφανίζεται ως περιοχή υψηλού σήματος. Στη μαγνητική φασματοσκοπία (MR spectroscopy) το Πολύμορφο Γλοιοβλάστωμα παρουσιάζει αύξηση στο λόγο χολίνης/κρεατίνης, αύξηση στην τιμή της λακτάσης και ελάττωση στην τιμή της Ν-ακετυλοασπαρτάσης. Τα παραπάνω χαρακτηριστικά μπορούν να διευκολύνουν στη διαφοροδιάγνωση από όγκους χαμηλότερης κακοήθειας, καθώς και από την νέκρωση μετά την ακτινοθεραπεία κατά την παρακολούθηση του ασθενούς.
Το Πολύμορφο Γλοιοβλάστωμα είναι για λόγους άγνωστους, πιο κοινό στους άνδρες (αναλογία ανδρών έναντι των γυναικών περίπου 3:2). Τα περισσότερα γλοιοβλαστώματα φαίνεται να είναι σποραδικά, χωρίς κάποια γενετική προδιάθεση. Δεν έχει βρεθεί κάποια σχέση του γλοιοβλαστώματος με το κάπνισμα, τη διατροφή, τα κινητά τηλέφωνα ή τα ηλεκτρομαγνητικά πεδία. Πρόσφατα, ανακαλύφθηκαν στοιχεία για ιογενή αίτια, πιθανώς από τον ιό SV40 (ιός του DNA) ή τον κυτταρομεγαλοϊό. Επίσης φαίνεται να υπάρχει μια μικρή σχέση μεταξύ γλοιοβλαστώματος και ιονίζουσας ακτινοβολίας. Πιστεύεται επίσης ότι ενδέχεται να σχετίζεται με το PVC (θερμοπλαστικό πολυμερές που χρησιμοποιείται ευρέως). Αναφορές έχουν γίνει και για ενδεχόμενη συσχέτιση των καρκίνων του εγκεφάλου με την έκθεση σε μόλυβδο στο περιβάλλον εργασίας.
Άλλοι "παράγοντες" κινδύνου που σχετίζονται με την εμφάνιση Πολύμορφου Γλοιοβλαστώματος είναι:
-Το φύλο: ελαφρώς πιο κοινό στους άνδρες,
-Η ηλικία: συνήθως ασθενείς άνω των 50 ετών,
-Η εθνικότητα: Καυκάσιοι, Λατίνοι, Ασιάτες,
-Ιστορικό νόσου από χαμηλού βαθμού αστροκύττωμα, το οποίο με την πάροδο του χρόνου μπορεί να εξελιχθεί σε Πολύμορφο Γλοιοβλάστωμα,
-Ιστορικό νόσου από ένα εκ των παρακάτω γενετικών νοσημάτων: Νευροϊνωμάτωση, Οζώδης Σκλήρυνση, ασθένεια Von Hippel-Lindau, σύνδρομο Li-Fraumeni, σύνδρομο Turcot.
Όπως φανερώνει το όνομά του, το πολύμορφο γλοιοβλάστωμα εμφανίζει σημαντική ποικιλομορφία. Ιστολογικά τα κύτταρα του Πολύμορφου Γλοιοβλαστώματος, είναι πυκνά αστροκυτταρικά που διηθούν διάχυτα τον εγκεφαλικό ιστό. Τα καρκινικά κύτταρα είναι πολύπλοκα, έχουν διογκωμένο κυτταρόπλασμα και πυρήνες χρωματίνης (πολυμορφικές). Η μιτωτική δραστηριότητα είναι αυξημένη, ο δείκτης πολλαπλασιασμού Ki-67 είναι περισσότερο από 20%. Παρουσιάζει μεγάλη κυτταροβρίθεια και αποτελείται από χαμηλής διαφοροποίησης, συχνά πολύμορφα, νεοπλασματικά κύτταρα, από μικρά έως γιγαντιαία, με σημαντική κυτταρική ατυπία και μεγάλη μιτωτική δραστηριότητα. Ο αριθμός των μιτώσεων διαφέρει από όγκο σε όγκο, αλλά και κατά περιοχή μέσα στον ίδιο όγκο. Συνήθως, η αστροκυτταρική προέλευσή του είναι εμφανής, αλλά σε ορισμένες περιπτώσεις είναι δυσδιάκριτη. Οι υπόστροφες και οι αγγειακές αλλοιώσεις αποτελούν σταθερό ιστολογικό εύρημα. Οι νεκρώσεις είναι απαραίτητο ιστοπαθολογικό εύρημα, με χαρακτηριστική πασσαλιδώδη διάταξη κυττάρων γύρω από αυτές και μέγεθος που ποικίλει. Συχνότατη είναι η υπερπλασία των τριχοειδών αγγείων και η υπερτροφία και υπερπλασία των ενδοθηλιακών κυττάρων. Κρίσιμης σημασίας για τη διάγνωση του γλοιοβλαστώματος (και τη διάκρισή του από αναπλαστικό αστροκύτωμα), σύμφωνα με την κατάταξη των όγκων του Παγκόσμιου Οργανισμού Υγείας, είναι η ανίχνευση νέκρωσης ή αγγειοβρίθειας.
Υπάρχουν τέσσερις υπότυποι του γλοιοβλαστώματος:
Υπάρχουν τέσσερις υπότυποι του γλοιοβλαστώματος:
-Ενενήντα επτά τοις εκατό των όγκων ανήκουν στον «κλασικό» υπότυπο, και φέρουν επιπλέον αντίγραφα γονιδίων του υποδοχέα επιδερμικού αυξητικού παράγοντα (EGFR), ενώ το γονίδιο ΤΡ53, που συχνά μεταλλάσσεται στα γλοιοβλάστωμα, σπάνια μεταλλάσσεται σε αυτόν τον υπότυπο.
-Σε αντίθεση, ο προνευρικός υπότυπος, συχνά, έχει υψηλά ποσοστά μεταβολών στο ΤΡ53, και το PDGFRA, το γονίδιο που κωδικοποιεί τον υποδοχέα του παράγοντα ανάπτυξης του α-τύπου αιμοπεταλίων και το IDHl, το γονίδιο που κωδικοποιεί την ισοκιτρική αφυδρογονάση-1.
-Ο μεσεγχυματικός υπότυπος χαρακτηρίζεται από υψηλά ποσοστά μεταλλάξεων ή άλλες μεταβολές στο NF1, το γονίδιο που κωδικοποιεί τη Νευροϊνωμάτωση τύπου 1 και λιγότερες μεταβολές στο γονίδιο EGFR και λιγότερη έκφραση του EGFR από τα άλλα είδη.
-Πολλές άλλες γενετικές αλλοιώσεις έχουν περιγραφεί σε γλοιοβλάστωμα, και η πλειοψηφία τους είναι συγκεντρωμένες σε τρεις οδούς: του Ρ53, του RB, και του PI3K/AKT. Τα γλοιοβλαστώματα έχουν μεταβολές στο 64-87%, 68-78% και 88% σε αυτές τις οδούς, αντίστοιχα. Μία άλλη σημαντική μεταβολή είναι η μεθυλίωση των MGMT, που είναι ένα ένζυμο επιδιόρθωσης του DNA. Η μεθυλίωση στη μεταγραφή του DNA και, επομένως, στην έκφραση του ενζύμου MGMT σχετίζεται με μια βελτιωμένη απόκριση στη θεραπεία με καταστροφή του DNA από χημειοθεραπευτικά, όπως η τεμοζολομίδη.
Τα καρκινικά βλαστικά κύτταρα-όπως έχουν βρεθεί σε γλοιοβλαστώματα είναι η αιτία της αντοχής σε συμβατικές θεραπείες, και το υψηλό ποσοστό επανεμφάνισης της νόσου.
Ένας βιοδείκτης για τα κύτταρα σε γλοιοβλαστώματα που εμφανίζουν ιδιότητες βλαστικών κυττάρων είναι ο παράγοντας μεταγραφής Hes3, που έχει δειχθεί ότι ρυθμίζει τον αριθμό τους όταν αυτά τοποθετούνται σε καλλιέργεια. Επιπλέον, το πολύμορφο γλοιοβλάστωμα παρουσιάζει πολλές διαφοροποιήσεις σε γονίδια που κωδικοποιούν για κανάλια ιόντων, συμπεριλαμβανομένων της υπερέκφραση των GBK διαύλων καλίου και των CLC-3 καναλιών χλωριδίου. Αυτά τα υπερδραστήρια κανάλια ιόντων, διευκολύνουν την αυξημένη κίνηση ιόντων των καρκινικών κυττάρων του γλοιοβλαστώματος, πάνω από την κυτταρική μεμβράνη, αυξάνοντας έτσι την κίνηση μέσω όσμωσης και την γρήγορη εξάπλωσή τους.
Λόγω ακριβώς της χαρακτηριστικής ιστοπαθολογίας του το Πολύμορφο Γλοιοβλάστωμα έχει χαρακτηριστικά ευρήματα και στον νευροαπεικονιστικό έλεγχο: η διάγνωσή του γίνεται με αξονική (CT) και μαγνητική τομογραφία (MRI) με την ταυτόχρονη χορήγηση σκιαγραφικού. Στην απεικόνιση CT με σκιαγραφικό, το γλοιοβλάστωμα εμφανίζεται ακανόνιστο σχήμα με δακτυλιοειδή ενίσχυση. Στην περιοχή γύρω από τον όγκο υπάρχει σημαντικό οίδημα. Τα ευρήματα της μαγνητικής τομογραφίας είναι αρκετά χαρακτηριστικά: ο όγκος έχει μεγάλη αντίθεση με το υγιές παρέγχυμα και υπάρχουν και αιμορραγικά στοιχεία και νεκρώσεις. Τελικά, η διάγνωση του όγκου γίνεται πάντα με βιοψία εγκεφάλου. Σε ορισμένες περιπτώσεις γίνεται ηλεκτροεγκεφαλογράφημα και οσφυονωτιαία παρακέντηση για να εκτιμηθεί η γενική κατάσταση και για διαφοροδιάγνωση από το απόστημα στον εγκέφαλο ή το λέμφωμα. Η εμφάνιση του Πολύμορφου Γλοιοβλαστώματος στον νευροαπεικονιστικό έλεγχο μπορεί να είναι μεν χαρακτηριστική δεν είναι όμως και συγκεκριμένη, καθώς και κάποιες άλλες αλλοιώσεις, όπως το απόστημα, η μετάσταση, η σκλήρυνση κατά πλάκας ενδέχεται να έχουν παρόμοια εμφάνιση. Η Μαγνητική Φασματοσκοπία (MR Spectroscopy) βοηθάει πάρα πολύ στην διάγνωση. Πιο συγκεκριμένα, με τη μαγνητική φασματοσκοπία δίδεται η δυνατότητα να χαρτογραφήσουμε τόσο τη χημική σύσταση, όσο και τη μεταβολική δραστηριότητα των ιστών των απεικονιζόμενων όγκων, λαμβάνοντας σημαντικές πληροφορίες όσον αφορά την ταυτοποίηση (τύπος βλάβης), τη σταδιοποίηση (βαθμός κακοήθειας), αλλά και τον καλύτερο σχεδιασμό της θεραπευτικής προσέγγισης βλαβών των διαφόρων ανατομικών περιοχών του εγκεφάλου. Επειδή όμως ο βαθμός ταξινόμησης του όγκου βασίζεται στο πλέον κακοήθες τμήμα του, η ολική εκτομή του όγκου ή κατευθυνόμενη μέσω νευροπλοήγησης βιοψία, είναι ο μόνος τρόπος ταυτοποίησής του και χάραξης της θεραπευτικής του αντιμετώπισης. Σε καμία περίπτωση η μαγνητική φασματοσκοπία δεν αντικαθιστά την ιστολογική επιβεβαίωση.
Στη θεραπευτική φαρέτρα για τους ασθενείς με πολύμορφο γλοιοβλάστωμα εμπεριέχονται η εγχείρηση, η ακτινοθεραπεία και η χημειοθεραπεία. Η κλασσική αντιμετώπιση συμπεριλαμβάνει και τις τρεις και συγκεκριμένα την μέγιστη χειρουργική εξαίρεση, ακολουθούμενη από μετεγχειρητική ακτινοθεραπεία, με την προσθήκη χημειοθεραπείας στην πλειονότητα των ασθενών.
Η θεραπεία των πρωτογενών όγκων του εγκεφάλου και των εγκεφαλικών μεταστάσεων διακρίνεται σε συμπτωματική και παρηγορητική θεραπεία. Η υποστηρικτική-συμπτωματική θεραπεία επικεντρώνεται στην ανακούφιση των συμπτωμάτων και τη βελτίωση της νευρολογικής λειτουργίας του ασθενούς. Οι πρωτογενείς υποστηρικτικοί θεραπευτικοί παράγοντες είναι τα αντιεπιληπτικά και τα κορτικοστεροειδή.
Το 90% περίπου των ασθενών με γλοιοβλάστωμα υποβάλλονται σε αντιεπιληπτική θεραπεία, αν και έχει εκτιμηθεί ότι μόνο περίπου το 40% των ασθενών απαιτούν αυτή τη θεραπεία. Πρόσφατα, έχει προταθεί ότι δεν απαιτείται η χορήγηση αντιεπιληπτικών προφυλακτικά, και θα πρέπει να υπάρξει πριν επιληπτική κρίση για τη συνταγογράφηση αυτού του φαρμάκου. Εκείνοι που λαμβάνουν ταυτόχρονα φαινυτοΐνη με την ακτινοβολία μπορεί να αναπτύξουν σοβαρές δερματικές αντιδράσεις όπως πολύμορφο ερύθημα και σύνδρομο Stevens-Johnson. Από τα κορτικοστεροειδή, συνήθως δίδεται δεξαμεθαζόνη 4 έως 8 mg κάθε 4 έως 6 ώρες, η οποία μπορεί να μειώσει το οίδημα γύρω από τον όγκο (μέσω της αναδιάταξης του φραγμού αίματος-εγκεφάλου), να μειώσει την ισχύ της μάζας και την ενδοκρανιακή πίεση, και να μειώσει την κεφαλαλγία ή την υπνηλία.
Το Πολύμορφο Γλοιοβλάστωμα χαρακτηρίζεται από πολύ φτωχή πρόγνωση, παρά την ύπαρξη πολλών θεραπευτικών μεθόδων, που περιλαμβάνουν την ανοικτή κρανιοτομία με χειρουργική εκτομή του μεγαλύτερου δυνατού τμήματος του όγκου, ακολουθούμενη από ταυτόχρονη ή επακόλουθη χημειοακτινοθεραπεία, αντιαγγειογενετική θεραπεία με μπεβασιζουμάμπη (bevacizumab-Avastin), ακτινοχειρουργική gamma knife ή cyber knife και συμπτωματική φροντίδα με κορτικοστεροειδή και αντιεπιληπτικά. Με εξαίρεση τα γλοιώματα του εγκεφαλικού στελέχους, έχει τη χειρότερη πρόγνωση από κάθε άλλη κακοήθεια του κεντρικού νευρικού συστήματος, με ενδιάμεση επιβίωση 14 μήνες.
Η θεραπεία των πρωτογενών όγκων του εγκεφάλου και των εγκεφαλικών μεταστάσεων διακρίνεται σε συμπτωματική και παρηγορητική θεραπεία. Η υποστηρικτική-συμπτωματική θεραπεία επικεντρώνεται στην ανακούφιση των συμπτωμάτων και τη βελτίωση της νευρολογικής λειτουργίας του ασθενούς. Οι πρωτογενείς υποστηρικτικοί θεραπευτικοί παράγοντες είναι τα αντιεπιληπτικά και τα κορτικοστεροειδή.
Το 90% περίπου των ασθενών με γλοιοβλάστωμα υποβάλλονται σε αντιεπιληπτική θεραπεία, αν και έχει εκτιμηθεί ότι μόνο περίπου το 40% των ασθενών απαιτούν αυτή τη θεραπεία. Πρόσφατα, έχει προταθεί ότι δεν απαιτείται η χορήγηση αντιεπιληπτικών προφυλακτικά, και θα πρέπει να υπάρξει πριν επιληπτική κρίση για τη συνταγογράφηση αυτού του φαρμάκου. Εκείνοι που λαμβάνουν ταυτόχρονα φαινυτοΐνη με την ακτινοβολία μπορεί να αναπτύξουν σοβαρές δερματικές αντιδράσεις όπως πολύμορφο ερύθημα και σύνδρομο Stevens-Johnson. Από τα κορτικοστεροειδή, συνήθως δίδεται δεξαμεθαζόνη 4 έως 8 mg κάθε 4 έως 6 ώρες, η οποία μπορεί να μειώσει το οίδημα γύρω από τον όγκο (μέσω της αναδιάταξης του φραγμού αίματος-εγκεφάλου), να μειώσει την ισχύ της μάζας και την ενδοκρανιακή πίεση, και να μειώσει την κεφαλαλγία ή την υπνηλία.
Το Πολύμορφο Γλοιοβλάστωμα χαρακτηρίζεται από πολύ φτωχή πρόγνωση, παρά την ύπαρξη πολλών θεραπευτικών μεθόδων, που περιλαμβάνουν την ανοικτή κρανιοτομία με χειρουργική εκτομή του μεγαλύτερου δυνατού τμήματος του όγκου, ακολουθούμενη από ταυτόχρονη ή επακόλουθη χημειοακτινοθεραπεία, αντιαγγειογενετική θεραπεία με μπεβασιζουμάμπη (bevacizumab-Avastin), ακτινοχειρουργική gamma knife ή cyber knife και συμπτωματική φροντίδα με κορτικοστεροειδή και αντιεπιληπτικά. Με εξαίρεση τα γλοιώματα του εγκεφαλικού στελέχους, έχει τη χειρότερη πρόγνωση από κάθε άλλη κακοήθεια του κεντρικού νευρικού συστήματος, με ενδιάμεση επιβίωση 14 μήνες.
Η εγχειρητική εξαίρεση αναλόγως της έκτασής της χαρακτηρίζεται ως πλήρης, υφολική, μερική εξαίρεση του όγκου. Ιδιαίτερη περίπτωση αποτελεί η στερεοτακτική βιοψία, η οποία εφαρμόζεται σε περιπτώσεις όγκων που προσπελαύνονται με δυσχέρεια ή ανεγχείρητων, με στόχο την ιστοπαθολογική τους ταυτοποίηση. Όλες οι παραπάνω έχουν στόχο τόσο την εκτομή ή την ογκομείωση και την αποσυμπίεση του εγκεφάλου, όσο και την λήψη ικανής ποσότητας ιστού για την παθολογοανατομική εξέταση. Προοπτικές μελέτες σε ασθενείς με κακόηθες γλοίωμα ανέδειξαν την μεγάλη προγνωστική σημασία της ευρείας εξαίρεσης σε σχέση με μόνη τη βιοψία. Οι περισσότερες μελέτες υποδεικνύουν ότι η έκταση της εξαίρεσης αποτελεί σημαντικό προγνωστικό παράγοντα. Η διάμεση επιβίωση για τους ασθενείς με περισσότερο από 70% εκτομή είναι 14,4 μήνες, σε σύγκριση με τους 10,5 μήνες για όσους ασθενείς έχουν 70% εκτομή ή λιγότερο. Η διάμεση επιβίωση για τους ασθενείς με υπολειπόμενο όγκο μικρότερο από 5 cm3 είναι 14,4 μήνες, ενώ η διάμεση επιβίωση για τους ασθενείς με μεγαλύτερο υπολειπόμενο όγκο δεν ξεπερνά τους 10,5 μήνες.
1. Ιστολογική ταυτοποιήση του όγκου.
2. Ανακούφιση του ασθενούς απο τα συμπτώματα.
3. Μείωση του συνολικού αριθμού των καρκινικών κυττάρων και
4. Συνέργεια με άλλες θεραπευτικές μεθόδους π.χ. χημειοθεραπεία, ακτινοθεραπεία, ανοσοθεραπεία.
Γενικώς, η ιδανική χειρουργικά επιλογή είναι η μέγιστη ασφαλής εξαίρεση, αυτή δηλαδή που δεν θα αφήσει βαριά νευρολογικά ελλείμματα στον ασθενή. O χρόνος και η ποιότητα της μετεγχειρητικής επιβίωσης είναι οι σπουδαιότεροι παράμετροι με τους οποίους αξιολογούμε τα αποτελέσματα κάθε θεραπείας για τους όγκους του εγκεφάλου. Η μετεγχειρητική θνητότητα για το κακόηθες γλοίωμα το 1960 ήταν μεταξύ 20%-40%. Μετά την εφαρμογή των κορτικοειδών και της προόδου της νευροαναισθησίας, η θνητότητα μειώθηκε στο 4% στην δεκαετία του 1970. Σήμερα με την χρήση της μικροχειρουργικής η θνητότητα είναι ~0,7%. Αυτή όμως η μείωση της μετεγχειρητικής θνητότητας δεν συμβαδίζει και με παράλληλη αύξηση του χρόνου επιβίωσης των ασθενών. Με βάση τις μελέτες του Frankel και German η ολική εξαίρεση του γλοιοβλαστώματος παρουσιάζει επιβίωση για 6 μήνες στο 45% των ασθενών, ενώ μόνο 20% των ασθενών είναι ζώντες μετά από μερική εξαίρεση του όγκου. Μετά από 1 χρόνο ζούσαν το 22% και το 7% αντίστοιχα των ασθενών. Οι Hitchcock και Sato παρουσιάζουν επιβίωση στο 76% των ασθενών για 6 μήνες, αλλά μόνο το 28% από αυτούς ήταν ικανοί να επιστρέψουν στην εργασία τους. Βέβαια εδώ πρέπει να λάβουμε υπ'οψη μας ότι υπάρχουν πολλοί παράγοντες οι οποίοι επηρεάζουν την μετεγχειρητική νευρολογική κατάσταση των ασθενών μεταξύ των οποίων συμπεριλαμβάνονται η οικογενειακή κατάσταση του πάσχοντος, οι κοινωνικές και ψυχολογικές επιρροές του, κ.α. Κατά την τελευταία δεκαετία έχει βελτιωθεί σημαντικά η ποιότητα ζωής αλλά και ο μέσος όρος επιβίωσης ασθενών με γλοιώματα. Αυτό οφείλεται στην εξάπλωση της εφαρμογής νέων τεχνικών, οι οποίες επιτρέπουν τη ριζικότερη αφαίρεση γλοιωμάτων ακόμα και σε ιδιαίτερα δυσπρόσιτες περιοχές του εγκεφάλου, προστατεύοντας συγχρόνως σημαντικά λειτουργικά κέντρα του. Οι τεχνικές αυτές είναι η νευροπλοήγηση, η λειτουργική μαγνητική τομογραφία, ο διεγχειρητικός νευροφυσιολογικός έλεγχος και η διεγχειρητική απεικόνιση μέσω υπερήχου ή ειδικών συστημάτων διεγχειρητικής μαγνητικής τομογραφίας. Σε κάποιες περιπτώσεις μερικοί ασθενείς επωφελούνται από την εμφύτευση τοπικής χημειοθεραπείας με πολυμερή καρμουστίνης. Σε ορισμένες περιπτώσεις ιδιαίτερα δυσμενούς πρόγνωσης, όπως διήθησης περισσοτέρων του ενός λοβών του εγκεφάλου, επέκτασης σε περιοχή λειτουργικών κέντρων (λόγου, βασικών γαγγλίων, στελέχους), η «ανοικτή» χειρουργική επέμβαση δεν προσφέρει ουσιαστικό όφελος, καθώς με αυτήν δεν πραγματοποιείται ριζική αφαίρεση του όγκου. Σε αυτήν την περίπτωση συνιστάται συνήθως επιβεβαίωση της διάγνωσης μέσω ιστολογικής εξέτασης, μετά τη λήψη στερεοτακτικής βιοψίας.
Η ακτινοθεραπεία ενδείκνυται σε όλες τις περιπτώσεις ασθενών με Πολύμορφο Γλοιοβλάστωμα και αποτελεί απαραίτητη μετεγχειρητική τακτική από δεκαετίες, καθώς τυχαιοποιημένες μελέτες και μετα-αναλύσεις δείχνουν αύξηση της επιβίωσης των ασθενών με την προσθήκη της, ανεξάρτητα από την έκταση της εγχείρησης (βιοψία, μερική ή ολική εξαίρεση). Παλαιότερα, στην ακτινοθεραπεία του Πολύμορφου Γλοιοβλαστώματος χρησιμοποιούνταν η ολοκρανιακή ακτινοβόληση που έδωσε τη θέση της στην μερική ακτινοβόληση του εγκεφάλου. Ο λόγος για την μείωση του μεγέθους των πεδίων ακτινοθεραπείας είναι ότι τα Πολύμορφα Γλοιοβλαστώματα στη συντριπτική τους πλειοψηφία υποτροπιάζουν τοπικά, εντός 2 cm από την αρχική τους θέση, ανεξάρτητα από το αν η ακτινοβόληση είναι ολοκρανιακή ή τοπική. Σε διάφορες τυχαιοποιημένες μελέτες δεν βρέθηκε διαφορά στην επιβίωση, ούτε στο χρόνο προόδου της νόσου μεταξύ της ολοκρανιακής και της εντοπισμένης ακτινοθεραπείας. Επιπρόσθετα, η εντοπισμένη ακτινοβόληση υπερέχει της ολοκρανιακής, λόγω της ελάττωσης των παρενεργειών, κυρίως των νευρολογικών, και της δυνατότητας αύξησης της δόσης. Με τη βελτίωση των μεθόδων απεικόνισης αλλά και των τεχνικών ακτινοθεραπείας, ακτινοβολείται πλέον μόνο η περιοχή του όγκου με την προσθήκη περιμετρικά ζώνης «υγιούς» εγκεφαλικού παρεγχύματος, σε μία ή συνηθέστερα δύο φάσεις με σταδιακά σμικρυνόμενα πεδία ανάλογα με το μέγεθος του ακτινοβολούμενου ιστού. Σήμερα, η γενικώς αποδεκτή δόση για το πολύμορφο γλοιοβλάστωμα βρίσκεται στην περιοχή των 60 Gy. Συγκεκριμένα, χορηγούνται 60 Gy σε 30 ημερήσιες συνεδρίες ή 59,4 Gy σε 33 συνεδρίες (ημερήσια δόση όγκου τα 2 ή 1,8 Gy, αντίστοιχα), μέσα φυσικά στα περιθώρια ανοχής των γύρω υγιών ιστών. Ένα συντομότερο σχήμα ακτινοθεραπείας, όπως 40 Gy σε 15 συνεδρίες σε διάστημα 3 εβδομάδων, μπορεί να χρησιμοποιηθεί σε ηλικιωμένους ασθενείς, με ισοδύναμα αποτελέσματα. Σε ασθενείς μεγαλύτερους των 65 ετών και λειτουργική κατάσταση κατά Karnofsky μικρότερη ή ίση του 50, η παρηγορική ακτινοθεραπεία με 30 Gy σε 10 συνεδρίες αποτελεί γενικά αποδεκτή τακτική.
Ο ρόλος της χημειοθεραπείας μετά την ακτινοθεραπεία ή μετά την χειρουργική επέμβαση σε ασθενείς με Πολύμορφο Γλοιοβλάστωμα, παρέμενε ασαφής για πολλά χρόνια. Οι περιορισμοί στη χρήση της χημειοθεραπείας στους όγκους του εγκεφάλου είναι: 1) η μικρή διείσδυση των φαρμάκων λόγω του αιματοεγκεφαλικού φραγμού, της υποξίας και της ενδοκράνιας πίεσης, 2) η συστηματική τοξικότητα (μυελοκαταστολή), 3) οι αλληλεπιδράσεις με φάρμακα που συχνά χορηγούνται σε ασθενείς με όγκους εγκεφάλου όπως για παράδειγμα τα αντιεπιληπτικά που επηρεάζουν την κάθαρση πακλιταξέλης και ιρινοτεκάνης μέσω αναστολής του κυτοχρώματος P-450 ή τα κορτικοστεροειδή που επηρεάζουν τα επίπεδα φαινυτοΐνης και 4) η ενδογενής αντίσταση των όγκων, όπως για παράδειγμα η αντίσταση στους αλκυλιωτικούς παράγοντες, σε περιπτώσεις κακοήθων γλοιωμάτων όταν τα επίπεδα της O6-alkylguanine DNA-alkyltransferase (AGAT) είναι υψηλά.
Στη βιβλιογραφία, τα αποτελέσματα για τα οφέλη της χημειοθεραπείας ήταν αμφιλεγόμενα, καθώς οι περισσότερες μελέτες έδειχναν στατιστικά μη σημαντική αύξηση της συνολικής επιβίωσης των ασθενών με την προσθήκη της χημειοθεραπείας. Οι Walker και συν. σε τυχαιοποιημένη μελέτη που πραγματοποίησαν, διαπίστωσαν μικρή και στατιστικώς μη σημαντική διαφορά στην επιβίωση με την προσθήκη νιτροζουρίας στην ακτινοθεραπεία. Ανάλογα, ούτε η μεγάλη τυχαιοποιημένη μελέτη του Medical Research Council έδειξε αύξηση της επιβίωσης με την προσθήκη χημειοθεραπείας με προκαρβαζίνη, λομουστίνη και βινκριστίνη (σχήμα PCV) στους ασθενείς με κακόηθες γλοίωμα. Αντίθετα με τις παραπάνω μελέτες, μία μετα-ανάλυση του Glioma Meta-analysis Trialists Group σε συνολικά 3004 ασθενών από 12 δημοσιευμένες τυχαιοποιημένες μελέτες, έδειξε ότι η προσθήκη της χημειοθεραπείας στην εγχείρηση και την ακτινοθεραπεία, προσφέρει μια μικρή (6%), αλλά στατιστικά σημαντική αύξηση, όσον αφορά το ποσοστό μονοετούς επιβίωσης και 2 μήνες αύξηση στη συνολική επιβίωση σε ασθενείς με κακόηθες γλοίωμα. Πρόσφατα, ένας νεότερος χημειοθεραπευτικός παράγοντας - η τεμοζολομίδη - αποτέλεσε αντικείμενο έρευνας, ως χημειοθεραπεία για πρωτοπαθείς όγκους του κεντρικού νευρικού συστήματος. Η τεμοζολομίδη (Temodal) αποτελεί ένα δεύτερης γενιάς αλκυλιωτικό παράγοντα που χορηγείται από του στόματος και έχει δείξει αποτελεσματικότητα στη θεραπεία μιας ποικιλίας νεοπλασμάτων, όπως το μελάνωμα και οι εγκεφαλικές μεταστάσεις, ενώ χρησιμοποιούνταν και για το υποτροπιάζον γλοιοβλάστωμα. Έχει συγκεκριμένα πλεονεκτήματα έναντι άλλων αλκυλιωτικών παραγόντων, λόγω της μοναδικής χημικής δομής και των φαρμακοκινητικών ιδιοτήτων αυτής. Λόγω του μικρού μοριακού βάρους της, η τεμοζολομίδη διαπερνά αποτελεσματικά τον αιματοεγκεφαλικό φραγμό και για το λόγο αυτό, θεωρείται ως ένας πολλά υποσχόμενος παράγοντας έναντι των πρωτοπαθών εγκεφαλικών όγκων και των δευτεροπαθών κακοηθειών του κεντρικού νευρικού συστήματος. Επιπρόσθετα, η τεμοζολομίδη χορηγείται από το στόμα χωρίς διαιτητικούς περιορισμούς και ουσιαστικά το 100% της εκ του στόματος χορηγούμενης δόσης εισέρχεται στο αίμα. Η τεμοζολομίδη είναι γενικώς ασφαλής και καλά ανεκτή από τους ασθενείς, καθώς σχετίζεται με χαμηλό ποσοστό εμφάνισης σοβαρών ανεπιθύμητων ενεργειών. Συχνότερες ανεπιθύμητες ενέργειες από τη χορήγησή της είναι: η ναυτία, ο έμετος, το αίσθημα κόπωσης, η υπνηλία και η αιματολογική τοξικότητα (κυρίως θρομβοπενία και λευκοπενία). Μια Ελληνική πολυκεντρική τυχαιοποιημένη μελέτη φάσεως ΙΙ σε 130 ασθενείς με ΠΓΒ που δημοσιεύτηκε πρόσφατα έδειξε ότι η προσθήκη της τεμοζολομίδης στη μετεγχειρητική ακτινοθεραπεία αυτών των ασθενών, υπερτερεί έναντι μόνης της ακτινοθεραπείας. Η υπεροχή της συνδυασμένης θεραπείας αφορούσε τόσο το χρόνο έως την πρόοδο της νόσου όσο και τη συνολική επιβίωση των ασθενών. Πρόσφατα, το 2005, η τεμοζολομίδη προστέθηκε ως βασική θεραπεία στην αντιμετώπιση των ασθενών με πρόσφατα διαγνωσμένο Πολύμορφο Γλοιοβλάστωμα σε συνδυασμό με τη μετεγχειρητική ακτινοθεραπεία. Στη μεγάλη τυχαιοποιημένη μελέτη της EORTC 26981 (European Organisation for Research and Treatment of Cancer), τυχαιοποιήθηκαν 573 ασθενείς με πρόσφατα διαγνωσμένο ΠΓΒ σε δύο σκέλη. Στο πρώτο σκέλος οι ασθενείς υποβλήθηκαν σε θεραπεία με τεμοζολομίδη ταυτόχρονα με την ακτινοθεραπεία (75 mg/m2 επιφάνειας σώματος καθημερινά έως το πέρας της ακτινοθεραπείας) και στη συνεχεία σε 6 κύκλους τεμοζολομίδης (150-200 mg/m2 επιφάνειας σώματος για πέντε συνεχόμενες ημέρες σε κύκλους των 28 ημερών), ενώ στο δεύτερο σκέλος υποβλήθηκαν μόνο σε ακτινοθεραπεία. Η συγκεκριμένη μελέτη, ανέδειξε στατιστικά σημαντική διαφορά στη συνολική διάμεση επιβίωση (14.6 μήνες vs 12.1 μήνες), καθώς και στο ποσοστό διετούς επιβίωσης (26% vs 10%) υπέρ των ασθενών που έλαβαν τεμοζολομίδη. Η αύξηση αυτή της επιβίωσης φαίνεται να είναι σημαντικότερη σε ασθενείς νέους και με καλή γενική κατάσταση.
Σημαντική έρευνα πραγματοποιείται τα τελευταία χρόνια σε σχέση με τη χρήση στοχευμένων φαρμάκων [αναστολείς EGFR (epidermal growth factor receptor), PDGFR (platelet-derived growth factor receptor), mTOR (mammalian target of rapamycin) και άλλα] και αντιαγγειογενετικών παραγόντων [Anti VEGF (Vascular endothelial growth factor)] στη θεραπεία των ασθενών με γλοιοβλάστωμα.
Ο συνδυασμός ακτινοθεραπείας (60 Gy μόνο στην περιοχή του όγκου) μαζί με τα χημειοθεραπευτικά φάρμακα τεμοζολαμίδη (Temodal) και λομουστίνη (CCNU) είναι σε θέση να αυξήσει ουσιαστικά τη διάρκεια επιβίωσης των ασθενών. Η συνήθης θεραπεία για το πολύμορφο γλοιοβλάστωμα που χρησιμοποιείται περισσότερο κατά τα τελευταία χρόνια είναι η ακτινοθεραπεία σε συνδυασμό με την τεμοζολαμίδη. Η προσθήκη της λομουστίνης φαίνεται ότι συμβάλλει σημαντικά στην επιβίωση των ασθενών.
Η μελέτη AVAglio, που παρουσιάστηκε πρόσφατα στο 17ο Ετήσιο Συνέδριο της Εταιρείας Νευρο-Ογκολογίας στις Η.Π.Α., είναι η πρώτη μελέτη φάσης III σε ασθενείς με νεοδιαγνωσθέν γλοιοβλάστωμα από το 2005, με θετικά αποτελέσματα σε ένα από τα κύρια καταληκτικά σημεία της, δηλαδή την επιβίωση χωρίς εξέλιξη της νόσου. Συγκεκριμένα, τα δεδομένα της μελέτης καταδεικνύουν ότι η μπεβασιζουμάμπη (Bevacizumab-Avastin) σε συνδυασμό με ακτινοθεραπεία και χημειοθεραπεία με τεμοζολομίδη μείωσε κατά 36% τον κίνδυνο εξέλιξης του καρκίνου ή θανάτου σε ασθενείς με νεοδιαγνωσθέν γλοιοβλάστωμα, σε σύγκριση με την ακτινοθεραπεία με τεμοζολομίδη και εικονικό φάρμακο. Η μείωση αυτή ισοδυναμεί με αύξηση της διάμεσης επιβίωσης των ασθενών χωρίς εξέλιξη της νόσου τους κατά 4,4 μήνες. Για το χρονικό διάστημα χωρίς εξέλιξη της νόσου, οι ασθενείς είχαν καταφέρει να διατηρήσουν τόσο τη λειτουργική τους ανεξαρτησία, όσο και έναν αριθμό σημαντικών παραμέτρων της ποιότητας ζωής τους. Ένα επιπρόσθετο όφελος ήταν ότι οι ασθενείς στο σκέλος που έλαβαν μπεβασιζουμάμπη χρειάστηκαν μικρότερη δόση κορτικοστεροειδών.
Μια αξιολόγηση της συνολικής επιβίωσης των ασθενών από ανεξάρτητη επιτροπή αναθεώρησης έδειξε επίσης 39% μείωση στον κίνδυνο εξέλιξης της νόσου ή θανάτου. Το ποσοστό επιβίωσης στον ένα χρόνο ήταν 72% για το σκέλος της μπεβασιζουμάμπης έναντι 66% για το σκέλος του εικονικού φαρμάκου. Οι ασθενείς με νεοδιαγνωσθέν γλοιοβλάστωμα έχουν λίγες θεραπευτικές επιλογές και υπάρχει μεγάλη ανάγκη για νέες φαρμακευτικές αγωγές κατά της νόσου. Οι όγκοι των ασθενών με γλοιοβλάστωμα χαρακτηρίζονται από πολύ υψηλά επίπεδα αγγειακού ενδοθηλιακού αυξητικού παράγοντα (VEGF) – από τα υψηλότερα που παρατηρούνται στους συμπαγείς όγκους. Για το λόγο αυτό το γλοιοβλάστωμα αποτελεί θεραπευτικό στόχο για τη μπεβασιζουμάμπη, καθώς η μπεβασιζουμάμπη αποτελεί μια αντι-αγγειογενετική θεραπεία που έχει την ιδιότητα να δεσμεύεται ειδικά και να αναστέλλει τις βιολογικές επιδράσεις του παράγοντα VEGF, βασικού ρυθμιστή της αγγειογένεσης των όγκων (μιας θεμελιώδους διαδικασίας προκειμένου ένας όγκος να κάνει μεταστάσεις σε άλλα μέρη του σώματος). Η αναστολή του σχηματισμού αυτών των νέων αιμοφόρων αγγείων στερεί από τον όγκο το απαραίτητο οξυγόνο και τα θρεπτικά συστατικά που χρειάζεται για να αναπτυχθεί και να εξαπλωθεί.
Ο συνδυασμός ακτινοθεραπείας (60 Gy μόνο στην περιοχή του όγκου) μαζί με τα χημειοθεραπευτικά φάρμακα τεμοζολαμίδη και λομουστίνη (CCNU) είναι σε θέση να αυξάνει ουσιαστικά τη διάρκεια επιβίωσης των ασθενών. Σε μια ενδιαφέρουσα θεραπευτική δοκιμή Γερμανοί γιατροί από το πανεπιστήμιο της Βόνης, χορήγησαν τον εν λόγω συνδυασμό σε 39 ασθενείς που είχαν μόλις διαγνωσθεί με πολύμορφο γλοιοβλάστωμα. Με τη συνήθη θεραπεία η διάρκεια επιβίωσης των ασθενών είναι κατά μέσο όρο 15 περίπου μήνες. Οι ασθενείς που έλαβαν ακτινοθεραπεία, τεμοζολαμίδη και λομουστίνη επιβίωσαν κατά μέσο όρο 23 μήνες. Αυτό σημαίνει ότι οι ασθενείς κέρδισαν κατά μέσο όρο 8 περίπου μήνες. Όμως μερικοί ασθενείς έζησαν για περισσότερο από 4 χρόνια. Σε μια μελέτη του 2009 μάλιστα αναφέρεται ότι σχεδόν το 10% των ασθενών με γλοιοβλάστωμα μπορεί να ζήσει πέντε χρόνια ή και περισσότερο. Τα παιδιά με όγκους υψηλού βαθμού κακοήθειας (βαθμούς III και IV) τείνουν να έχουν πολύ καλύτερη πρόγνωση από τους ενήλικες από τους ενήλικες: η πενταετής επιβίωση για τα παιδιά είναι περίπου 25%. Εξίσου σχετικά καλύτερη πρόγνωση έχουν και οι ασθενείς με γλοίωμα Στελέχους.
Το πολύμορφο γλοιοβλάστωμα, λόγω του έντονα διηθητικού χαρακτήρα, αποτελεί τον πιο κακοήθη από τους όγκους του εγκεφάλου και υποτροπιάζει τοπικά σε σύντομο χρονικό διάστημα. Η πρόγνωση των ασθενών με πολύμορφο γλοιοβλάστωμα είναι κάκιστη, με διάμεση επιβίωση τριών μηνών, σε αυτούς που δεν λαμβάνουν καμία θεραπεία (χειρουργική επέμβαση, ακτινοθεραπεία ή χημειοθεραπεία).
Παρά την βελτίωση των τεχνικών στην νευροχειρουργική και την ακτινοθεραπεία και τους νέους χημειοθεραπευτικούς παράγοντες, η διάμεση επιβίωση των ασθενών με πολύμορφο γλοιοβλάστωμα παραμένει χαμηλή, στους 10-12 μήνες, ενώ μόνο ένα ποσοστό περίπου 15% επιζεί πέραν της διετίας από την αρχική διάγνωση. Η σχετικά καλύτερη διάμεση επιβίωση που αναφέρεται σε πολλές από τις τυχαιοποιημένες μελέτες, οφείλεται στην επιλογή των ασθενών, οι οποίοι συνήθως ανήκουν σε προγνωστικά καλύτερες υποομάδες (νεότερη ηλικία, βελτιωμένη κλινική κατάσταση κ.λ.π.). Σε ανασκόπηση του German Glioma Network αναφέρεται ότι ένας στους είκοσι ασθενείς επιβιώνει πέραν της τριετίας και ένας στους 5000 πέραν τις δεκαετίας. Οι κλινικές παράμετροι που αναγνωρίζονται από τις περισσότερες μελέτες της διεθνούς βιβλιογραφίας ως προγνωστικοί παράγοντες για τους ασθενείς με πολύμορφο γλοιοβλάστωμα είναι η ηλικία, η λειτουργική κατάσταση του ασθενούς (performance status) και η έκταση της χειρουργικής εξαίρεσης.
Η χειρουργική επέμβαση είναι το πρώτο στάδιο της θεραπείας του γλοιοβλαστώματος.
Παρά την βελτίωση των τεχνικών στην νευροχειρουργική και την ακτινοθεραπεία και τους νέους χημειοθεραπευτικούς παράγοντες, η διάμεση επιβίωση των ασθενών με πολύμορφο γλοιοβλάστωμα παραμένει χαμηλή, στους 10-12 μήνες, ενώ μόνο ένα ποσοστό περίπου 15% επιζεί πέραν της διετίας από την αρχική διάγνωση. Η σχετικά καλύτερη διάμεση επιβίωση που αναφέρεται σε πολλές από τις τυχαιοποιημένες μελέτες, οφείλεται στην επιλογή των ασθενών, οι οποίοι συνήθως ανήκουν σε προγνωστικά καλύτερες υποομάδες (νεότερη ηλικία, βελτιωμένη κλινική κατάσταση κ.λ.π.). Σε ανασκόπηση του German Glioma Network αναφέρεται ότι ένας στους είκοσι ασθενείς επιβιώνει πέραν της τριετίας και ένας στους 5000 πέραν τις δεκαετίας. Οι κλινικές παράμετροι που αναγνωρίζονται από τις περισσότερες μελέτες της διεθνούς βιβλιογραφίας ως προγνωστικοί παράγοντες για τους ασθενείς με πολύμορφο γλοιοβλάστωμα είναι η ηλικία, η λειτουργική κατάσταση του ασθενούς (performance status) και η έκταση της χειρουργικής εξαίρεσης.
Η χειρουργική επέμβαση είναι το πρώτο στάδιο της θεραπείας του γλοιοβλαστώματος.
Χρησιμοποιείται: α) για να ληφθεί ένα τμήμα του όγκου για ιστολογική ταυτοποίηση και διάγνωση, β) για την μείωση των συμπτωμάτων πίεσης από μια μεγάλη μάζα που πιέζει τον εγκέφαλο, γ) για την απομάκρυνση της νόσου πριν από την θεραπεία με ακτινοθεραπεία και χημειοθεραπεία, και δ) για να παρατείνει την επιβίωση των ασθενών. Όσο μεγαλύτερη είναι η έκταση της απομάκρυνσης του όγκου, τόσο το καλύτερο. Αφαίρεση του 98% ή περισσότερο του όγκου έχει συσχετιστεί με ένα σημαντικά μεγαλύτερο χρόνο επιβίωσης. Οι πιθανότητες σχεδόν πλήρους αφαίρεσης του όγκου μπορεί να αυξηθούν σημαντικά εάν η χειρουργική επέμβαση καθοδηγείται από μια φθορίζουσα χρωστική ουσία γνωστή ως 5-αμινολεβουλινικό οξύ.
Ακτινοβολία χρησιμοποιείται μετά από χειρουργική επέμβαση σε μια προσπάθεια να κατασταλεί η νόσος και να ανασταλεί η υποτροπή της. Μετά τη χειρουργική επέμβαση, η ακτινοθεραπεία είναι ο στυλοβάτης της θεραπείας για τα άτομα με γλοιοβλάστωμα. Η ολοκρανιακή ακτινοθεραπεία εγκεφάλου δεν είναι καλύτερη σε σύγκριση με την πιο ακριβή και στοχευμένη τρισδιάστατη σύμμορφη ακτινοθεραπεία. Μία συνολική δόση ακτινοβολίας 60-65 Gy έχει βρεθεί να είναι η καλύτερη για τη θεραπεία. Σε άλλες μορφές καρκίνου, όπου ακτινοβολία μπορεί να παρατείνει την επιβίωση ή ακόμη και να θεραπεύσει όγκους, η προσθήκη της χημειοθεραπείας στην ακτινοβολία βελτιώνει την επιβίωση σε σχέση με την ακτινοβολία μόνο. Παραδείγματα περιλαμβάνουν ο καρκίνος του τραχήλου της μήτρας, ο καρκίνος του φάρυγγα και άλλα. Οι περισσότερες μελέτες για το πολύμορφο γλοιοβλάστωμα δεν έδειξαν όφελος από την προσθήκη της χημειοθεραπείας. Ωστόσο, μια μεγάλη κλινική δοκιμή με 575 συμμετέχοντες έδειξε ότι η τεμοζολομίδη φαίνεται να ευαισθητοποιεί τα κυττάρα του όγκου στην ακτινοβολία. Οι υψηλές δόσεις τεμοζολομίδης δεν έχει πρόσθετο όφελος. Η Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων ενέκρινε το Avastin (bevacizumab) για τη θεραπεία ασθενών με γλοιοβλάστωμα σε εξέλιξη μετά από καθιερωμένη θεραπεία με βάση τα αποτελέσματα των δύο μελετών που έδειξαν ότι το Avastin μειώνει το μέγεθος του όγκου σε ορισμένους ασθενείς με γλοιοβλάστωμα. Στην πρώτη μελέτη, 28% των ασθενών με γλοιοβλάστωμα είχαν συρρίκνωση του όγκου, 38% επιβίωσαν για τουλάχιστον ένα έτος, και 43% επιβίωσαν για τουλάχιστον έξι μήνες χωρίς εξέλιξη της νόσου τους. Σε αντίθεση με την περίπτωση για τον καρκίνο του παχέος εντέρου, τον καρκίνο του πνεύμονα και άλλες μορφές καρκίνου, όπου η bevacizumab ενισχύει τη χημειοθεραπεία, στο πολύμορφο γλοιοβλάστωμα η προσθήκη της χημειοθεραπείας στη bevacizumab δεν βελτιώσε τα αποτελέσματα, σε σχέση με την bevacizumab μόνο. Η Bevacizumab ελαττώνει το οίδημα του εγκεφάλου και τα συμπτώματα. Μερικοί ασθενείς με εγκεφαλικό οίδημα δεν έχουν στην πραγματικότητα ενεργό όγκο, αλλά μάλλον τα συμπτώματα οφείλονται στην ανάπτυξη του οιδήματος ως καθυστερημένη επίδραση της προηγούμενης θεραπείας με ακτινοβολία. Αυτό το είδος του οιδήματος είναι δύσκολο να διακριθεί το οίδημα του όγκου, γιατί αυτά μπορεί να συνυπάρχουν. Και τα δύο ανταποκρίνονται στη bevacizumab.
Φαίνεται ότι ορισμένες αλλαγές στα γονίδια (γονότυπος) των ασθενών έχουν καθοριστικό ρόλο στην επιτυχία της θεραπείας. Σε 11 ασθενείς που έλαβαν το νέο συνδυασμό, είχε βρεθεί μια συγκεκριμένη αλλοίωση σε ένα γονίδιο (O6-methylguanine–DNA methyltransferase, MGMT gene promotor methylation). Οι ασθενείς αυτοί είχαν σημαντικά μεγαλύτερο χρόνο επιβίωσης που ήταν κατά μέσο όρο 34 μήνες. Στους υπόλοιπους ασθενείς η προσθήκη της τεμοζολαμίδης και της λομουστίνης στις δόσεις που χρησιμοποιήθηκαν δεν φάνηκε να προσφέρει σημαντικά στο χρόνο επιβίωσης σε σύγκριση με το τι προσφέρει σε ανάλογους ασθενείς η χορήγηση της ακτινοθεραπείας μόνο. Έτσι με τη διενέργεια ενός μόνο τεστ για το συγκεκριμένο γονίδιο αποφασίζεται εάν η επιπρόσθετη χημειοθεραπεία με τα δύο αυτά φάρμακα θα μπορεί να προσφέρει ή όχι αύξηση της επιβίωσης στους ασθενείς με πολύμορφο γλοιοβλάστωμα.
Όπως αναφέρουν σύγχρονες μελέτες, δύο πρόσφατα αναγνωρισθέντα γονίδια -C/EPB και Stat3- προκαλούν μικρή βλάβη μεμονωμένα, αλλά η συνεργασία τους όταν είναι και τα δύο ενεργά έχει καταστροφικά αποτελέσματα, ενεργοποιώντας εκατοντάδες άλλα γονίδια και οι ασθενείς αυτοί εμφανίζουν πολύ κακή πρόγνωση. Το ελπιδοφόρο είναι ότι η απενεργοποίηση των δύο αυτών γονιδίων σε κύτταρα ανθρώπινων εγκεφαλικών όγκων τα κατέστησε ανίκανα να σχηματίσουν όγκους όταν χορηγήθηκαν σε ποντίκια.
Γενετικές ανωμαλίες που συνδέονται με το γλοιοβλάστωμα είναι μεταλλάξεις ογκοκατασταλτικών γονιδίων TP53 ( χρωμόσωμα 17 ), του ρετινοβλαστώματος κατασταλτικό γονίδιο RB-1 ( χρωμόσωμα 13 ) και οι απώλειες του χρωμοσώματος 22 και η πλήρης απώλεια του χρωμοσώματος 10 . Αυτές οι γενετικές ανωμαλίες είναι συχνά παρούσες σε συνδυασμούς. Σε ασθενείς μεγαλύτερης ηλικίας είναι πιο συχνή η απώλεια του PTEN γονιδίου ή η ενίσχυση του EGFR γονιδίου. Στους μεσήλικες συχνές είναι οι μεταλλάξεις του TP53 γονιδίου. Επιπλέον, γίνεται φανερό ότι οι μεταλλάξεις σημείο της isocitrate αφυδρογονάσης IDH1 γονιδίου σε αυτή την ομάδα είναι πιο συχνές. Το σπάνιο γλοιοβλάστωμα της παιδικής ηλικίας διαφέρει στις γενετικές αλλαγές.
Τα τελευταία χρόνια τα βλαστικά κύτταρα μονοπωλούν το ενδιαφέρον περισσότερο από κάθε άλλο πεδίο στη βιολογία. Αυτό συμβαίνει γιατί η αποκάλυψη και η αποκωδικοποίηση των μοναδικών ιδιοτήτων τους αναμένεται να βοηθήσει στην κατανόηση των βιολογικών μηχανισμών των κυττάρων και παράλληλα να οδηγήσει στην ανεύρεση δυνητικών θεραπειών με εφαρμογή στα εκφυλιστικά νοσήματα και την αναγεννητική ιατρική. Έτσι αναμένεται η χρησιμοποίηση των βλαστικών κυττάρων για τη θεραπεία του πρωτοπαθούς καρκίνου του εγκεφάλου και συγκεκριμένα η θεραπεία με στόχο τα βλαστικά κύτταρα, η θεραπεία με μονοκλωνικά αντισώματα και η ογκολυτική θεραπεία με ιούς. Εκτιμάται ότι τα βλαστικά κύτταρα θα βοηθήσουν στις γνώσεις μας για την πρόκληση του πρωτοπαθούς καρκίνου του εγκεφάλου και την θεραπεία του.
Η ανάπτυξη νέων θεραπειών για το γλοιοβλάστωμα αποτελεί αντικείμενο της εντατικής έρευνας. Σε συνδυασμό με την τεμοζολομίδη, επί του παρόντος σε φάση ΙΙΙ κλινική δοκιμή του φαρμάκου Cilengitide (σιλενγιτίδη) δοκιμάζεται. Τα αποτελέσματα δείχνουν μια βελτίωση της αποτελεσματικότητας της ακτινοβολίας και της χημειοθεραπεία για να με μικρό επιπλέον επιβάρυνση για τον οργανισμό. Η επιτυχία της θεραπείας εξαρτάται από την μεθλίωση του MGMT υποκινητή γονιδίου. Οι υποδοχείς τυροσίνης κινάσης, ο υποδοχέας επιδερμικού αυξητικού παράγοντα του (EGFR) και ο αυξητικός παράγοντας αιμοπεταλίων (PDGF) αποτελούν πιθανούς στόχους για νέες θεραπευτικές προσεγγίσεις. Η θεραπεία σε κλινικές δοκιμές με μπεβασιζουμάμπη, σε συνδυασμό με τον αναστολέα τοποϊσομεράσης την ιρινοτεκάνη, δείχνουν ότι μειώνουν την επέκταση και ορισμένες ομάδες ασθενών μπορεί να ανταποκριθούν πολύ θετικά σε αυτή τη θεραπεία.
Από τις αρχές του 2010, ξεκίνησε μια τυχαιοποιημένη κλινική μελέτη φάσης ΙΙ σε γλοιοβλαστώματα με το νέο φάρμακο πρωτεΐνη-APG101. Εδώ, η αποτελεσματικότητα της θεραπείας, που αποτελείται από ακτινοθεραπεία και ενδοφλέβια χορήγηση της APG101 συγκρίνεται με ακτινοθεραπεία μόνο. Η APG101 είναι μια CD95-FC πρωτεΐνη σύντηξης για την αντιμετώπιση των κακοηθών νόσων. Η APG101 είναι μια νέα προσέγγιση για τη θεραπεία του γλοιοβλαστώματος και με αυτή επιδιώκεται, να αποφευχθεί η περαιτέρω ανάπτυξη του γλοιοβλαστώματος. Αυτή η θεραπεία βασίζεται σε ευρήματα από το Γερμανικό Κέντρο Έρευνας για τον Καρκίνο (DKFZ), σε κύτταρα γλοιοβλαστώματος καθώς διεγείρει την σύνδεση του CD95 προσδέτη στον υποδοχέα CD95, κι έτσι σταματάει η ανάπτυξη των καρκινικών κυττάρων. Μέχρι στιγμής η APG101 δοκιμάστηκε σε 20 υγιείς εθελοντές και 32 ασθενείς, ήταν καλά ανεκτή χωρίς σοβαρές παρενέργειες. Επίσης, δοκιμάζεται σε κλινικές δοκιμές, κι ένα νέο φάρμακο το Enzastaurinum (bisindolylmaleimide).
Μια άλλη προσέγγιση είναι η πειραματική θεραπεία με νανοσωματίδια. Αυτά αποτελούνται από ένα πυρήνα οξείδιου του σιδήρου και ένα κέλυφος, το οποίο διευκολύνει τη διείσδυση των σωματιδίων οξειδίου του σιδήρου στα κύτταρα του καρκίνου. Τα σωματίδια εισάγονται άμεσα στον όγκο με έγχυση. Στη συνέχεια γίνεται θέρμανση του οξειδίου του σιδήρου που είναι στον όγκο με εναλλασσόμενα μαγνητικά πεδία στους 46 ° C. Μια άλλη μελέτη με εμβόλιο με parvovirus είναι επίσης σε εξέλιξη.
Το Γλοιοβλάστωμα είναι εξαιρετικά δύσκολο να αντιμετωπιστεί. Η βέλτιστη ιατρική θεραπεία με χειρουργική επέμβαση και στη συνέχεια ακτινοβολία και χημειοθεραπεία, σύμφωνα με τις τρέχουσες μελέτες, παρατείνει το μέσο χρόνο επιβίωσης κατά αρκετούς μήνες και ανακουφίζει από τα συμπτώματα. Η διάμεση επιβίωση των ασθενών με γλοιοβλάστωμα είναι ~ 12 μήνες. Ωστόσο, το 3-5% των ασθενών επιβιώνει για περισσότερο από 3 χρόνια και αναφέρονται ως μακροχρόνια επιζώντες. Τα κλινικά δεδομένα και οι μοριακοί παράγοντες που συμβάλλουν στην μακροπρόθεσμη επιβίωση είναι ακόμα υπό διερεύνηση. Όμως κανείς ασθενής δεν πρέπει να θεωρείται "χαμένος" εκ των προτέρων. Το γεγονός και μόνο ότι τουλάχιστον 3 ασθενείς στους 100 πάσχοντες από Πολύμορφο Γλοιοβλάστωμα καταφέρνουν να επιζήσουν 3 χρόνια και σε γενικά καλή νευρολογική κατάσταση, είναι μία ένδειξη πως ο χρόνος τελικά είναι προς όφελος των ασθενών και σε βάρος του καρκίνου. Με τους ρυθμούς που εξελίσσεται σήμερα η επιστήμη κανείς δεν μπορεί να προβλέψει την πρόοδο που θα επιτελεστεί στα επόμενα χρόνια.